①据摩熵数据显示,2023年利多卡因凝胶贴膏在国内医院和药店的销售额合计超1.13亿元; ②在利多卡因凝胶贴膏撤回之前,华纳药厂在2025年已撤回两款药品的注册申请。
《科创板日报》1月27日讯(记者 史士云)今日晚间,华纳药厂(688799.SH)发布公告称,国家药监局已同意公司撤回利多卡因凝胶贴膏的注册申请(注册分类属于化学药品4类)。华纳药厂曾于2025年3月提交了该产品的上市申请。

对于撤回的原因,华纳药厂称是经审慎研究,结合研发策略所作出的决定,系主动撤回,并称此次撤回不会对公司当期及未来生产经营与业绩产生重大影响。
资料显示,利多卡因凝胶贴膏原研由日本Teikoku Seiyaku公司开发,其是一种局部外用的酰胺类局麻药,作用机制是通过皮肤渗透发挥局部镇痛作用,是临床常用的外用止痛药物,主要用于缓解无破损皮肤的带状疱疹后神经痛。据摩熵数据显示,2023年该产品在国内医院和药店的销售额合计超1.13亿元。
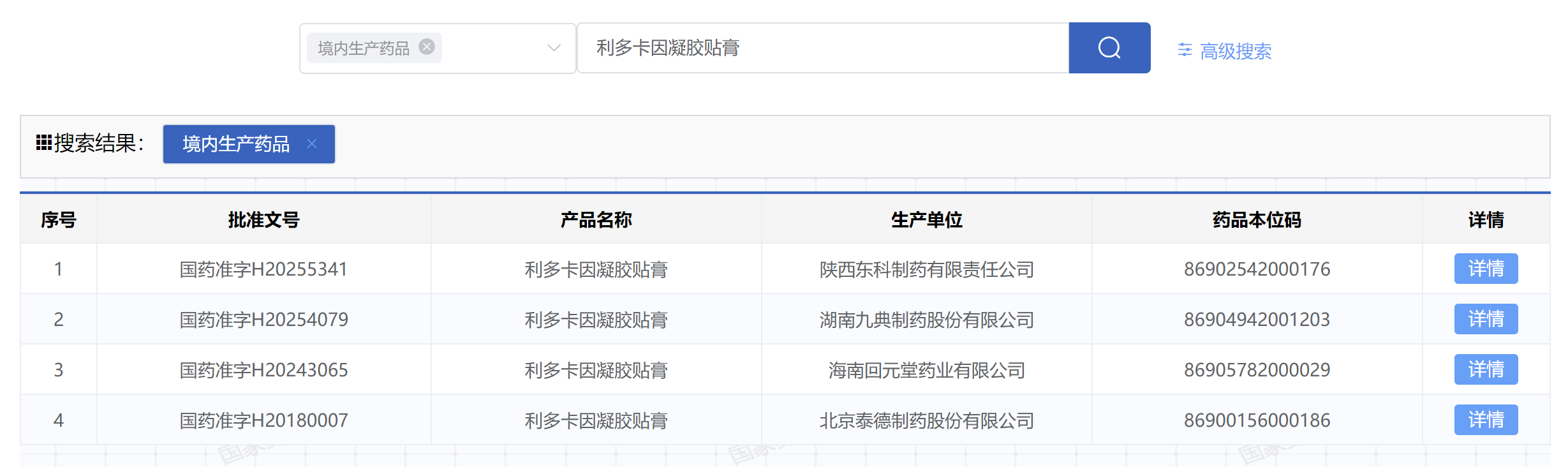
另据国家药监局官网信息,原研利多卡因凝胶贴膏于2024年5月获批进入中国市场,同时,国内还有四款利多卡因凝胶贴膏仿制药获批,涉及企业包括九典制药、海南回元堂药业、东科制药、泰德制药等。
其中,曾率先拿下首仿的泰德制药利多卡因凝胶贴膏(商品名得百宁)于2025年获批了新适应症,用于缓解糖尿病性周围神经病理性疼痛(DPNP)治疗,成为全球首个、国内唯一获批DPNP治疗的贴剂药物。
值得关注的是,《科创板日报》记者梳理发现,在利多卡因凝胶贴膏撤回之前,华纳药厂在2025年已经撤回了两款药品的注册申请。
2025年10月,华纳药厂撤回了品盐酸阿罗洛尔片的注册申请,该产品主要用于治疗原发性高血压、心绞痛、原发性震颤等;12月,又宣布撤回西甲硅油乳剂的注册申请,该主要用于治疗由胃肠道中聚集了过多气体而引起的不适症状,如腹胀等,也可作为腹部影像学检查的辅助用药。至于撤回理由,与撤回利多卡因凝胶贴膏的原因一致。
华纳药厂成立于2001年,主营业务是化学原料药、化学药制剂和中药制剂的研发、生产与销售,产品涉及消化、呼吸、抗感染药等多个治疗领域。另据华纳药厂2025年的半年报披露,其还在创新药板块布局了中药、化药小分子、以及改良型新药三条管线,并已有多个项目进入临床试验阶段。
业绩表现方面,2025年前三季度,华纳药厂实现营收10.9亿元,同比增长1.55%;归母净利润达2.07亿元,同比增长30.75%,不过扣非归母净利润有所下滑,同比下降26.52%,为9884.17万元。
拉长时间线来看,华纳药厂自2021年科创板上市至2023年,业绩一直保持着较为稳定的增长。但从2024年开始,该公司营收、归母净利润同比双双下滑,降幅分别为1.38%、22.24%,业绩下滑的核心原因之一指向制剂营销中心,该板块受吸入用乙酰半胱氨酸溶液、磷霉素氨丁三醇散等产品参与区域联盟集采后价格下调的影响,业务表现承压,进而拖累了整体业绩。
截至目前,华纳药厂已有超20款产品被纳入了集采。
在 2025 年第十一批药品集采中,华纳药厂的盐酸贝尼地平片以 7.19 元/盒的价格中标,供应区域涵盖福建、浙江、湖北、宁夏、海南五地。
此外,华纳药厂还在拓展新的增长曲线。2025年10月,其发起设立湖南弗米探针生物科技有限公司,该公司注册资本5000万元,华纳药厂持股 47.50%,其主营业务为新型显影剂等产品的研发与开发。











